
PRACTICA XI
REACCIONES DE CARBOHIDRATOS
I. OBJETIVOS
II. MATERIAL
|
8 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
2 |
III. SUSTANCIAS
|
5 ml |
|
||
|
10 ml |
|
10 ml |
|
|
1 ml |
|
10 ml |
|
|
10 ml |
|
10 ml |
|
|
10 ml |
|
10 ml |
|
|
5 ml |
|||
|
5 ml |
|
15 ml |
|
IV. INFORMACION
Los azúcares o carbohidratos pueden ser monosacáridos, disacáridos, trisacáridos, oligosacáridos y polisacáridos.
Los monosacáridos reaccionan de acuerdo a los grupos hidroxilo y carbonilo que poseen.
Los disacáridos y los polisacáridos se pueden hidrolizar para producir monosacáridos.
Los azúcares que dan resultados positivos con las soluciones de Tollens, Benedict ó Fehling se conocen como azúcares reductores, y todos los carbohidratos que contienen un grupo hemiacetal o hemicetal dan pruebas positivas. Los carbohidratos que solo contienen grupos acetal o cetal no dan pruebas positivas con estas soluciones y se llaman azúcares no reductores.

La solución de Benedict se utiliza en la determinación cuantitativa de glucosa en la sangre.
Las osazonas de los mono y disacáridos son compuestos amarillos, que cristalizan en formas características de la solución en que se produce. Tienen puntos de fusión característicos. Todos los azúcares epímeros, que difieren en la configuración del C-2 , forman la misma osazona. Los monosacáridos forman precipitado en caliente y los disacáridos no. La glucosazona precipita en 2-3 minutos. En una suspensión del producto de reacción se observan con el microscopio haces de cristales amarillos. El campo de la xilosazona se ve como cristales largos amontonados. La arabinosazona se presenta como cristales amarillos agrupados en roseta.
V. PROCEDIMIENTO
Prueba de Tollens.
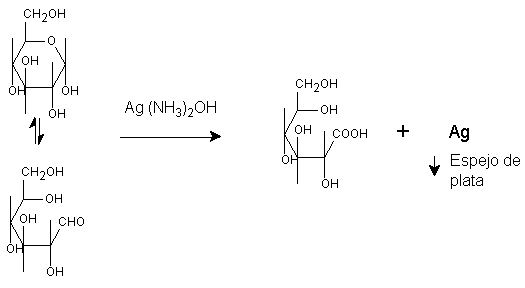
Procedimiento
Coloque en un tubo de ensayo limpio 1 ml de solución de nitrato de plata al 2.5%, agregue una gota de hidróxido de sodio al 5% y después gota a gota y con agitación una solución de hidróxido de amonio al 5% justo hasta que se disuelva el óxido de plata que precipitó, evitando cualquier exceso de NH4OH. Este reactivo debe usarse recién preparado y debe destruirse con un exceso de ácido nítrico al terminar de utilizarlo, ya que forma compuestos explosivos.
Agregue al reactivo recién preparado 5 a 10 gotas de solución de azúcar, agite y caliente brevemente en baño maría, sin dejar de agitar durante el calentamiento. La aparición de un espejo de plata indica prueba positiva para azúcar reductor. Una vez terminada la prueba el tubo de ensaye se deberá limpiar con ácido nítrico para destruir el espejo de plata.
Prueba de Fehling.
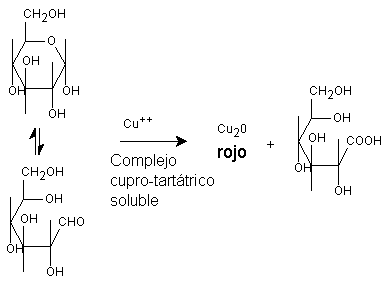
Procedimiento
Mezcle 1 ml de solución A y 1 ml de solución B, agregue dos o tres gotas de la solución del azúcar, caliente a ebullición.
La formación de un precipitado rojo y la decoloración de la solución indica prueba positiva para azúcar reductor.
Prueba de Benedict.
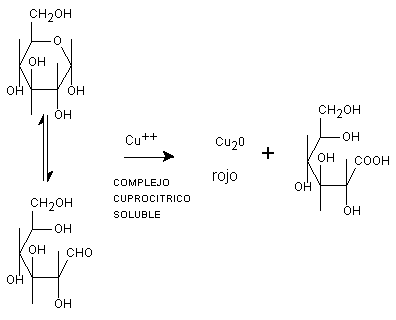
Procedimiento.
Coloque en un tubo de ensaye 1 ml del reactivo de Benedict y cuatro o cinco gotas de la solución del azúcar. Caliente a ebullición y deje enfriar a temperatura ambiente. Un precipitado cuya coloración varía desde amarillo hasta rojo, con decoloración de la solución, indica prueba positiva.
Anote los resultados en el siguiente cuadro:
|
Reacción de Tollens |
Reacción de Fehling |
Reacción de Benedict |
|
|
Glucosa |
|||
|
Fructuosa |
|||
|
Manosa |
|||
|
Sacarosa |
Formación de osazonas.
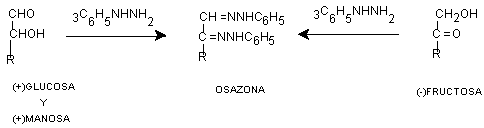
Procedimiento
Coloque en un tubo de ensaye limpio10 gotas de la solución del azucar,y agregue 1.5 ml de la solución de fenilhidrazina. Caliente la mezcla en baño de agua durante 10-20 minutos.
Filtre los cristales y observelos en un microscopio de bajo poder y determine su punto de fusión. El tiempo de formación de la ozasona y la apariencia de los cristales será diferente para los distintos azúcares.
Anote los resultados en el cuadro siguiente:
|
Tiempo de formación |
Apariencia de los cristales en el microscopio |
Punto de fusión |
|
|
Glucosa |
|||
|
Fructuosa |
|||
|
Manosa |
VI. ANTECEDENTES
a) Estructuras de los principales monosacáridos.
b) Reacciones de oxidación de los monoscáridos.
c) Reacción de los monosacáridos con fenilhidrazina ( osazonas).
d) Caracterización indirecta de azúcares a través de la formación de osazonas.
e) ¿Que se entiende por epímero?
e) Propiedades físicas, químicas y toxicidad de reactivos y productos.
VII. CUESTIONARIO
1) ¿ Por qué se considera reductor un azúcar?.
2) ¿En que consisten las pruebas que nos permiten saber si un azúcar es reductor?.
3) Escriba la reacción de cada una de las pruebas efectuadas en la práctica.
4) ¿Se puede desechar libremente en el derenaje los efluentes líquidos obtenidos en cada prueba? Diga que tratamiento se les deberá dar en cada caso para desecharlos al drenaje.
5) ¿Porqué no se deben tirar las sales de plata al drenaje?
ESPECTROS DE I.R.
A) GLUCOSA
B) FRUCTUOSA
C)MANOSA
VIII. BIBLIOGRAFIA
a) Moore J.A. y Dalrymple D.L.
Experimetal Methods in Organic Chemistry
5a. Edition
W.B. Saunders Co.
U.S.A. (1976)
pag 259-269.
b) Jacobs T.L., Truce W.E. y Robertson G. Ross
Laboratory Practice of Organic Chemistry
5a. Ed.
MacMilla Pub. Co. Inc.
U.S.A. (1974)
pag 311-316.
c)Hudlicky M.
Laboratory Experimetns in Organic Chemistry
3a. Ed.
Avery Publishing Group Inc.
U.S.A. (1985)
pag 104-106.
d)Daniels, Rush, Baver
J. Chem Ed. 1960, 37, 203.
e) Streitwieser A., Heathcok H.C.
Introduction to Organic Chemistry
MacMillan Pub. Co. Inc.
U.S.A. (1976)
pag 693-732.
f) Domínguez , Xorge A.
Métodos de Invstigación Fitoquímica
Editorial Limusa
México (1973)
Pag. 205