PRACTICA VIII
CONDENSACION DE CLAISEN-SCHMIDT
OBTENCION
DE DIBENZALACETONA
I. OBJETIVOS
a) Efectuar una condensación aldólica mixta.
b) Obtener un producto de uso comercial.
REACCION
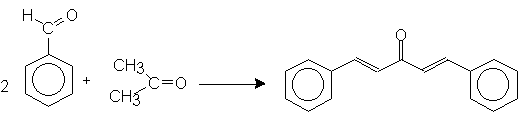
II. MATERIAL
|
1 |
|
1 |
|
2 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 1 1 |
|
1 2 2 |
III.
SUSTANCIAS
|
1.25 g |
|
70 ml |
|
1.25 g |
|
8 ml |
|
10 ml |
|
0.01g |
|
2 g |
|
3 ml |
IV.
INFORMACION
a)
Los aldehídos y las cetonas con hidrogenos unidos al carbono alfa al carbonilo
sufren reacciones de condensación aldólica.
b)
Los hidrógenos unidos al carbono alfa al carbonilo son hidrógenos ácidos.
c)
Las condensaciones aldólicas mixtas producen una mezcla de productos.
d)
Las reacciones de condensación entre cetonas y aldehídos no enolizables
producen un solo producto.
e)
Los productos obtenidos por condensación aldólica sufren reacciones de
crotonización.
f) La acetona no se polimeriza pero se
condensa en condiciones especiales dando productos que pueden considerarse como
derivados por eliminación.
V.
PROCEDIMIENTO
Coloque
en un matraz Erlenmeyer de 125 ml 1.25 g de NaOH, 12.5 ml de agua y 10 ml de
etanol. Posteriormente, agregue poco a poco y agitando 1.25 ml de benzaldehído
y luego 0.5 ml de acetona. Continue la agitación durante 20-30 minutos más,
manteniendo la temperatura entre 20-25o C mediante baños de agua fría.
Filtre
el precipitado, lave con agua fría, seque, recristalice de etanol (Nota 1).
Pese, determine punto de fusión y cromatoplaca comparando contra materia prima
el producto.
Datos cromatoplaca
Suspensión:
Gel de sílice al 35% en CHCl3/MeOH o en acetato de etilo.
Disolvente:
Acetona o acetato de etilo
Eluyente:
Hexano/Acetona 3:1
Revelador:
I2 o luz U.V.
NOTA
1) Si al recristalizar la solución se torna de un color rojo- naranja, puede que se encuentre demasiado alcalina, por lo que será necesario agregar ácido clorhídrico diluido 1:1, hasta que se tenga un pH entre 7 y 8.
VI. ANTECEDENTES
a) Reacciones de
condensación aldólica.
b) Reacciones de
condensación aldólica mixta.
· c) Otros ejemplos de reacciones de condensación de
Claisen- Schmidt.
d) Usos de la
dibenzalacetona
e) Propiedades
físicas, químicas y toxicidad de los reactivos y productos.
VII. CUESTIONARIO.
1) Explique por
qué debe adicionar primero benzaldehido y después la acetona a la mezcla de la
reacción.
2) Explique
porqué se obtiene un solo producto y no una mezcla de productos en esta
práctica.
3) Indique por
qué se crotoniza fácilmente el aldol producido.
4) ¿Por qué la
solución no debe estar alcalina al recristalizar?
5) Asigne las
bandas principales a los grupos funcionales presentes en los espectros de I.R.
de reactivos y productos.
Espectros de
I.R.
VIII.
BIBLIOGRAFIA
a) Vogel
A.I.
Elementary Practical Organic Chemistry
Part I, Small Scale Preparations
2nd. Edit.
Longman, London (1967)
pag 327
b) Conar C.R. and Dolliver M.A.
Org. Syn. Coll, 2,167 (1943)
John Wiley and Sons Inc.
c) Cremlyn R.J.W. and Still R.H.
Named and Miscellaneous Reactions in Organic Chemistry
Heinman Educational Books Ltd
London (1967)
d) Journal of Organic Chemistry 1962,27,327-328