




Traslapamiento de los orbitales p del acetileno.
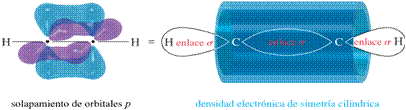
Del Traslapamiento de los dos orbitales p sin hibridar que quedan en cada átomo de carbono se forman dos orbitales pi. Estos
orbitales que forman un ángulo recto entre ellos se solapan dando lugar a dos enlaces pi, uno tiene su
mayor densidad electrónica
por encima y por debajo del enlace sigma C-C, y el otro tiene su mayor densidad electrónica por delante y por detrás
del enlace sigma. La distribución de densidad electrónica de estos dos enlaces pi en el acetileno tiene
simetría cilíndrica, de forma
que la densidad electrónica p rodea cilíndricamente al enlace sigma
entre los dos átomos de
carbono.
Cada átomo de carbono en el acetileno tiene dos
orbitales p sin hibridar con un electrón no enlazante. Es el solapamiento de los orbitales paralelos p el que forma el triple enlace (2 orbitales pi).