

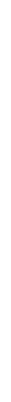
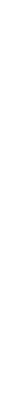



Estructuras del etileno y del etano
—Cada uno de los enlaces
carbono-hidrógeno está formado por el solapamiento de un orbital híbrido sp2 del carbono con el orbital 1s del átomo de hidrógeno. La longitud del enlace C-H en el etileno (1.08 Å) es ligeramente
más corta que la del enlace C-H en el etano (1.09 Å), ya que el orbital sp2 en el etileno tiene más carácter s (1/3 de s) que un orbital sp3 (1/4 de s). El orbital s está más próximo al núcleo que el orbital p, contribuyendo a acortar los enlaces
—El carbono sp3 tiene una geometría tetraédrica con ángulos
de 109.5°.
Los carbonos de enlace doble tienen hibridación sp2, por lo que tienen una geometría trigonal con ángulos de
casi 120°.
El solapamiento de los orbitales p sin hibridar
acorta la distancia
entre los carbonos desde 1.54A en alcanos hasta 1.33A en alcanos