




Efecto de las ramificaciones en el punto
de ebullición.
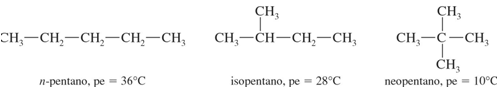
Se muestran los puntos de ebullición de tres isómeros de fórmula
molecular C5H12. El isómero de cadena
larga (n-pentano) es el
que tiene mayor área superficial y el punto de ebullición más alto. A medida que las ramificaciones de la cadena
aumentan, las moléculas se
hacen más esféricas y su área superficial disminuye. El isómero que tiene más ramificaciones (neopentano) tiene el área superficial más pequeña
y el punto de ebullición más
bajo.
Las áreas de mayor superficie en la molécula son idóneas para las
fuerzas de dispersión de London. Las
ramificaciones en una molécula reducirán su área de superficie, disminuyendo la cantidad de fuerzas de dispersión de
London. Los hidrocarburos
tienden a tener puntos de ebullición más elevados que sus isómeros ramificados debido a este motivo.