




Efecto de la estabilización por
resonancia sobre la fuerza ácida de
algunos compuestos orgánicos frecuentes.
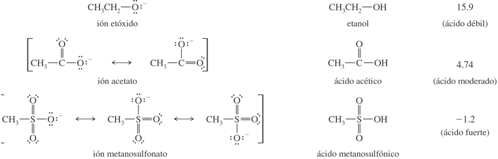
Estabilización por resonancia. La carga negativa de una
base conjugada puede estar deslocalizada entre dos o más átomos, y estabilizada por
resonancia. Dependiendo de la electronegatividad
que tengan esos átomos y de cómo se comparta esa carga, la deslocalización por resonancia con frecuencia es el efecto dominante en
la estabilización de un anión. Observe las bases conjugadas siguientes. El etóxido tiene una
carga negativa localizada en un átomo de oxígeno; el ión acetato tiene una carga negativa
compartida por dos átomos de oxígeno y el ión metanosulfonato tiene una carga negativa extendida
sobre tres átomos de oxígeno. Los ácidos conjugados de esos aniones muestran que los ácidos son
más fuertes si su desprotonación da lugar
a bases conjugadas estabilizadas por resonancia.