




Escala de electronegatividad de Pauling.
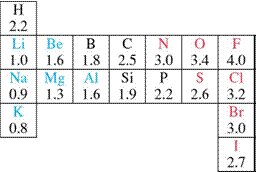
La electronegatividad es una guía para predecir la naturaleza polar
de los enlaces y la dirección del
momento dipolar. Cuanto más electronegativo sea el átomo, más "arrastrarán" los átomos a los electrones enlazantes hacia
ellos. El elemento más electronegativo
de la tabla periódica es el flúor, con un valor de electronegatividad de Pauling de 4,0. Aunque el carbono tiene una electronegatividad
ligeramente más elevada que el
hidrógeno, un enlace C-H se considera no polar a efectos prácticos.