Página principal http://organica1.org
9 Sustitución
nucleofílica alifática.
Nucleófilos y grupos
salientes
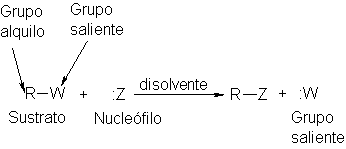
Los componentes requeridos para la sustitución nucleofílica son: sustrato, nucleófilo y disolvente. El
sustrato consta de dos partes: grupo
alquilo y grupo saliente. Nos ocuparemos del grupo alquilo durante gran
parte de este capítulo; estudiaremos las funciones del disolvente en el
capítulo 6. Por el momento examinaremos los otros componentes de estos
sistemas: los nucleófilos y grupos salientes.
Ya hemos visto lo suficiente para darnos cuenta de que la basicidad
tiene un lugar importante en la comprensión de los nucleófilos y de los grupos
salientes. Los nucleófilos se caracterizan por ser bases, y los grupos
salientes, por ser bases débiles.
Podemos encontrar una correlación aproximada entre grado de basidad, por una parte,
y poder nucleófilo o capacidad de salida, por otra: entre dos bases, la
de mayor poder nucleofilico es, a menudo, la más fuerte, mientras que
corrientemente el mejor grupo saliente es la base más débil. Sin embargo, esto sólo se cumple para
conjuntos de nucleófilos o de grupos salientes estrechamente relacionados:
aquellos que, entre otras cosas,
implican un mecanismo elemento central oxígeno, por ejemplo, o
nitrógeno. Hay muchas excepciones a tales correlaciones, siendo, evidentemente,
la basicidad sólo uno de los factores
involucrados.
Debemos comprender con claridad la diferencia entre basicidad y poder nucleofílico o capacidad de salida.
Todas tienen que ver con la tendencia o, en el caso de la capacidad de salida,
con la falta de tendencia a compartir un
par de electrones para formar un enlace covalente. Sin embargo, hay dos
diferencias fundamentales:
(a)
La basicidad es una
cuestión de equilibrio; el poder
nucleofílico y la tendencia a salir son cuestiones de velocidad. De dos bases, se dice
que una es más fuerte porque, en equilibrio, fija una mayor proporción
del ácido. De dos nucleófilos, el más poderoso es el que ataca más velozmente al carbono; de dos grupos
salientes, se dice que uno es mejor que el otro, porque abandonada más velozmente al carbono.
(b)
La basicidad (en el
sentido de Lowry-Bronsted) implica una interacción con un protón; el poder
nucleofílico y la capacidad de salida implican interacciones con el carbono.
Muchos de los productos que se
forman no son nuevos, pero por ahora sólo necesitamos apreciar cómo la
estructura de un producto en particular es el resultado natural de la
estructura de un determinado nucleófilo. Por el momento, utilizaremos
halogenuros de alquilo como ejemplos de sustratos.
Algunos nucleófilos son aniones, como el ión hidróxido;
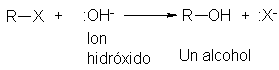
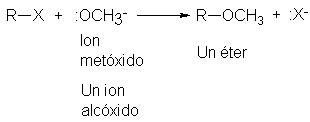
Los alcóxidos estrechamente
relacionados, como el metóxido;
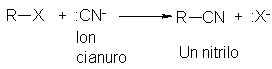
Cianuro (el anión fuertemente básico de un ácido muy débil, HCN);
O incluso otro ión halogenuro que,
aun siendo sólo débilmente básico, tiene un par de electrones no compartidos:
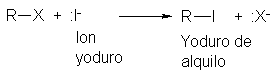
Pero las moléculas neutras también pueden poseer electrones no
compartidos, ser básicas y, en consecuencia, actuar como nucleófilos. El agua, por ejemplo, es capaz de atacar
un halogenuro de alquilo para dar, finalmente, un alcohol. El oxígeno del agua
ya tiene dos hidrógenos, de manera que cuando se liga al carbono, inicialmente
no se forma el alcohol
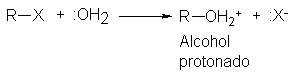
Mismo, sino ácido conjugado, es decir, el alcohol protonado; éste se transforma con facilidad en el alcohol por pérdida del protón.
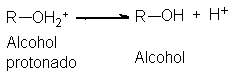
Aquí surge un aspecto importante. A menudo señalaremos por conveniencia la pérdida o
ganancia de un ión hidrógeno, H+, pero debe tenerse presente que no
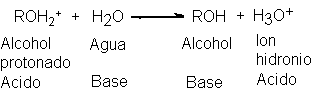
estamos realmente en presencia de un protón desnudo, sino que estamos más bien transfiriendo un protón de una base a
otra. En este caso, por ejemplo, se convierte el alcohol protonado en alcohol por
la transferencia del protón al agua, casi tan básica como el propio alcohol y
mucho más abundante.
Observemos ahora algunos de los grupos
salientes que encontraremos. Hasta aquí hemos empleado como ejemplos
principales los halogenuros de alquilo y continuaremos haciéndolo en las
secciones siguientes. Sin embargo, debemos considerar que estas reacciones
tienen lugar exactamente de la misma forma con otros sustratos: compuestos que
contienen, al igual que los halogenuros, grupos salientes muy buenos.
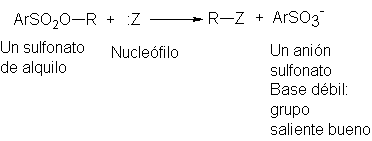
De estos otros sustratos, en lugar de los halogenuros de alquilo se
utilizan más corrientemente los alquil ésteres de ácidos sulfónicos, ArSO2OR:
sobre todo en el estudio de mecanismos de reacciones, pero también en síntesis.
Los ácidos sulfónicos, ArSO3H, están relacionados con el ácido
sulfúrico y como éste son ácidos fuertes.
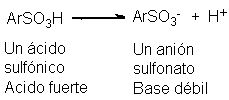
Sus aniones, los sulfonatos, son bases débiles y, en consecuencia,
grupos salientes buenos:
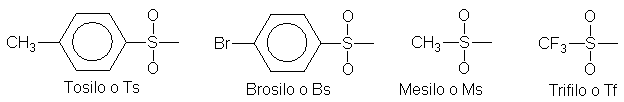
Los ésteres del ácido p-toluenosulfónico son los más empleados: los
p-toluenosulfonatos.
(Comprenderemos las estructuras de estos compuestos aromáticos más
adelante; por ahora basta con saber que se trata de grupos salientes buenos.)
El nombre del grupo p-toluenosulfonato suele abreviarse a tosilo (Ts), con lo que los p-toluenosulfonatos se convierten en tosilatos (TsOR).
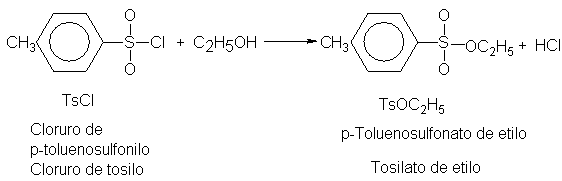
Al igual que los halogenuros de alquilo, los sulfonatos de alquilo
también se preparan con facilidad a partir de alcoholes. Por ejemplo:
En la sección 18.5 veremos que las dos síntesis difieren en un aspecto
muy importante.
Comencemos ahora nuestro estudio del mecanismo de la sustitución nucleofílica
alifática. Esta reacción ha fascinado a los químicos durante generaciones,
incluidos muchos de los <<famosos>>, cuyos nombres son o nos
llegarán a ser familiares: J.A. LeBel, G.N. Lewis, T. M. Lowry; y aquel gigante
de la química orgánica, Emil Fischer, que abrió los dos campos vastísimos de
los hidratos de carbono y las proteínas.
En la actualidad, el área de la química orgánica más ampliamente
estudiada es la sustitución nucleofílica alifática en sus diversas formas y
también la más polémica. La fascinación y el argumento se centra en dos
cuestiones relacionadas. El enlace del grupo saliente se está destruyendo, y el
del nucleófilo se está formando. (a) ¿Cuál es la regulación en el tiempo de estos dos procesos? (b) ¿De dónde
procede al energía requerida para la ruptura del enlace con el grupo saliente?
Comenzaremos el estudio del mecanismo en el punto donde comienza la
historia moderna de la reacción: con la cinética
de la sustitución nucleofílica alifática. Pero, antes de nada, ¿qué es la
cinética?