Página principal http://organica1.org
5 Alcoholes: breve introducción
Nos podemos avanzar mucho en la química orgánica de la mayoría de los
grupos sin encontrarnos con otra familia de compuestos: los alcoholes. La química de los halogenuros de alquilo no es la excepción.
Para comenzar, los alcoholes son las sustancias a partir de las cuales
casi siempre se forman los halogenuros
de alquilo, y de hecho la mayoría de los compuestos que sufren sustitución nucleofílica. Ahora bien, una vez
que se obtienen halogenuros de alquilo y se someten a sustitución nucleofílica,
nuevamente nos encontramos con los alcoholes desempeñando gran variedad de
papeles: pueden ser los reactivos con los cuales reaccionan los halogenuros de
alquilo, los productos o los disolventes en los que tiene lugar la reacción.
(De hecho, veremos que la preparación de halogenuros de alquilo involucra
también sustitución nucleofílica, esta vez con alcoholes como reactivos
sometidos a sustitución.)
Más adelante estudiaremos sistemáticamente la química de los alcoholes
(Caps. 17 y 18), pero por ahora aprenderemos justo lo suficiente sobre estos
compuestos para poder trabajar con ellos.
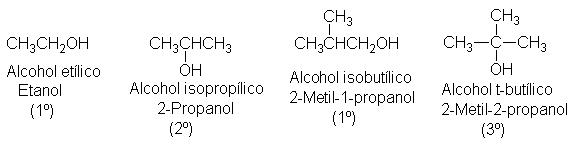
Los alcoholes son compuestos de fórmula general R-OH, donde R es
cualquier grupo alquilo y OH es el grupo hidroxilo. Un alcohol simple puede
nombrarse dando el nombre del grupo alquilo que está unido al grupo hidroxilo
con la terminación ílico, precedido de la palabra alcohol. Los nombres IUPAC se derivan agregando una letra l final
al nombre del alcano correspondiente. (Esta, nomenclatura se trata
detalladamente en la Sec. 17.4, que puede consultarse si se considera
necesario.) Al igual que un halogenuro de alquilo, un alcohol se clasifica como
primario, secundario o terciario,
según el tipo de carbono que lleva el grupo OH.
Entre las propiedades de los alcoholes, destaca un par de ellas que
debemos conocer: su acidez y su basicidad.
Estas propiedades residen en el grupo hidroxilo, OH, el grupo funcional de los
alcoholes. Este grupo es similar al grupo hidroxilo del agua, un compuesto que
ya nos resulta familiar. Los alcoholes, al igual que el agua, son ácidos y
bases débiles, casi tan ácidos y tan básicos como el agua.
Lo mismo que el agua, los alcoholes son lo suficientemente ácidos como
para reaccionar con metales activos, liberando hidrógeno gaseoso
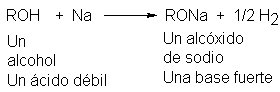
Los productos formados se llaman alcóxidos:
por ejemplo, etóxido de sodio o n-propóxido de potasio. Los alcóxidos son bases
fuertes, al igual que el hidróxido de sodio.
Al igual que el agua, también los alcoholes son lo suficientemente
básicos como para aceptar un protón de ácidos fuertes como el cloruro y el
sulfato de hidrógeno, permitiendo así la disociación completa de estas
sustancias, por ejemplo: