Página principal http://organica1.org
18 Estructura de carbocationes
En un carbocatión, el carbono deficiente en electrones se halla
enlazado a otros tres átomos mediante orbitales sp2. Estos orbitales
se encuentran en un plano, el del núcleo del carbono, y están dirigidos hacia
los vértices de un triángulo equilátero.
Esta parte del carbocatión es, en consecuencia, plana, con el carbono deficiente electrónicamente y los tres átomos
unidos a él ubicados en el mismo plano (Fig. 5.7a).
Sin embargo, la descripción de la molécula aún no está completa. El
carbono todavía posee un orbital p, con sus dos lóbulos ubicados por encima y
por debajo del plano de los enlaces o (Fig. 5.7b); en un carbocatión, este
orbital p se encuentra vacío. A pesar
de estar formalmente vacío, descubriremos que este orbital p está íntimamente
implicado en la química de los carbocationes: en sus estabilidades y en las
estabilidades de los diversos estados de transición que conducen a su formación. Este es el resultado del
solapamiento del orbital p con
otros orbitales cercanos solapamiento
geométricamente posible por la planaridad del carbocatión.
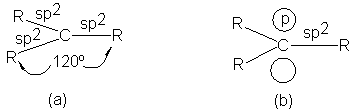
No cabe duda acerca de la planaridad de los carbocationes. La
descripción mecanico-cuántica de un carbocatión es exactamente la misma que la
del trifluoruro de boro (Sección 1.10), una molécula cuya planaridad está
firmemente establecida. Los espectros
RMN e infrarrojos de los carbocationes estabilizados, estudiados por Olah, son
consistentes con la hibridación sp2 y la planaridad: especialmente
los espectros infrarrojo y Raman del catión t-butilo son sorprendentemente
similares a los del trimetilboro, el cual se sabe que es plano.