Página principal http://organica1.org
1 Química homolítica y
heterolítica
Como ciencia, la química debe su existencia,
por supuesto, al cambio químico: la conversión de una sustancia en otra.
Moléculas antiguas son transformadas en otras nuevas, lo cual significa que deben
romperse enlaces antiguos para generar otros nuevos; en su mayoría enlaces
covalentes, en lo que respecta a la química orgánica.
Hemos visto que la ruptura de un enlace covalente puede ocurrir de dos
maneras fundamentalmente diferentes, dependiendo de lo que suceda con los dos
electrones que forman el par enlazante: en la homólisis, va un electrón a cada
fragmento; en la heterólisis, van ambos electrones al mismo fragmento. Los
sustantivos <<homólisis>> y heterólisis sólo se utilizan en su
sentido literal, para indicar la ruptura de enlaces. No obstante, los adjetivos
<<homolítico>> y <<heterolítico>> a falta de términos
más adecuados se emplean en un sentido más general, para incluir también el
proceso de la construcción de enlaces, pudiéndose definir así dos clases muy
amplias de reacciones orgánicas.
Por consiguiente, las reacciones homolíticas son aquellas en las que se quitan o se
proporcionan los electrones del par enlazante individualmente, tanto si se rompen enlaces,
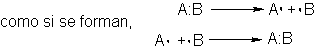
O si se rompen y forman simultáneamente,
![]()
Cada uno de los átomos que se separan lleva
uno de los electrones enlazantes, y cada
uno de los átomos que se juntan, proporciona uno de los electrones de enlace.
Reaccciones
heterolíticas son aquellas
en las cuales los electrones enlazantes se quitan o se proporcionan en pares. Tanto si se rompen enlaces.
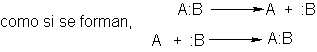
O si se rompen y forman simultáneamente,
![]()
Uno de los átomos que se separa lleva ambos
electrones de enlace, y uno de los átomos que se une proporciona el par.
.La química homolítica es, por tanto, la
química del electrón impar, mientras que la química heterolítica es la del par
de electrones. Mientras la primera se ocupa de partículas neutras, conocidas
como radicales libes, la segunda tiene que ver con cargas positivas y
negativas, es decir, con cationes y aniones. Las reacciones homolíticas suelen
producirse en la fase gaseosa, o en disolventes cuya función principal se reduce a proporcionar un medio
inerte que permita el movimiento libre de moléculas reaccionantes. Las
reacciones heterolíticas se realizan
generalmente en solución, y los disolventes tienen, como veremos, efectos muy
poderosos; la magnitud de su poder está empezando a conocerse ahora.
Hasta aquí, la reacción que más nos ha venido ocupando la sustitución
de radicales, ilustrada por la halogenación de los alcanos forma parte de la
química homolítica.
Comencemos ahora el estudio de la química heterolítica. La mayor parte de la química orgánica es heterolítica, siendo ésta la que más trataremos en el resto del libro. Tal como sucede con la halogenación, la reacción con la que empezamos es una sustitución, pero de un tipo muy diferente: es heterolítica y del tipo específico llamado sustitución nucleofílica alifática.