Página principal http://organica1.org
5
Preparación de éteres.
Síntesis de Williamson
En
laboratorio, la síntesis de
Williamson para éteres
es importante por
su versatilidad: puede
emplearse tanto para
obtener éteres simétricos
como asimétricos.
En la
síntesis de Wllamson
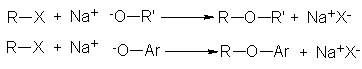
se hace reaccionar
un halogenuro de
alquilo ( halgenuro
de alquilio sustituido)
con un alcóxido
o un fenóxido
de sodio:
Para la
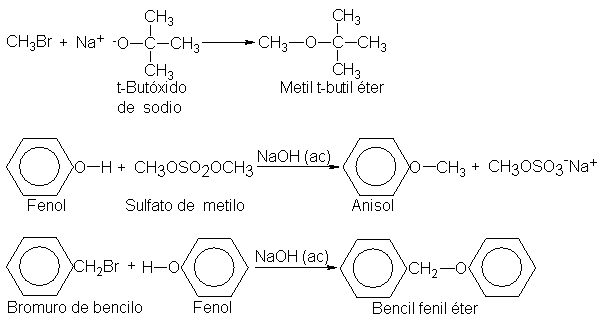
preparacón de aril metil éteres se suele utilizar sulfato de metilo, (CH3)2SO4,
en lugar de los mucho más caros
halogenuros de alquilo.
La síntesis
de Wlliamson implica
la sustitución nucleofílca
de un ion
alcóxido o fenóxido por un ion
halogenuro, y es
estrictamente análoga a
la preparación de alcoholes por
tratamiento de halogenuros
de alquilo con
hidróxido acuoso. En general
no pueden utilizarse
los halogenuros de
arilo, debido a
su poca reactividad
hacia la sustitución
nucleofílica.
Los alcóxidos
de sodio se obtienen
por acción directa
del sodio metálico
sobre alcoholes secos:
![]()
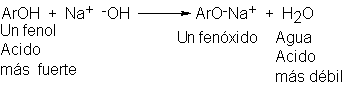
Por otra
parte, debido a la
apreciable acidez de los fenoles,
los fenóxidos de sodio se preparan por la acción del hidróxido de sodio acuoso sobre fenoles:
Si se
desea obtener un éter
dialquílico asimétrico, podemos
elegir entre dos
combinaciones de reactivos; una de
ellas es casi
siempre superior a
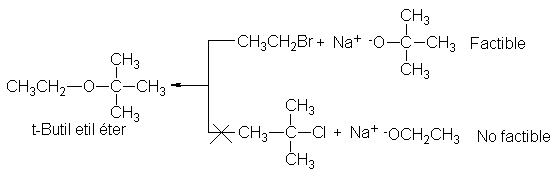
la otra. En
la preparación del
t-butil etil éter,
por ejemplo, son
lógicas las combinaciones
siguientes:
¿Cuál
elegimos? Como siempre,
consideremos el peligro
de una competencia de la elminación con
la sustitución deseada; en
este caso, la
elminación debe ser particularmente seria,
debido a la
fuerte basicidad del
alcóxido. Por consiguiente, descartaremos el uso
de un halogenuro
terciario, que debe
dar principalmente o
en su totalidad
el producto de la
elminación; debemos emplear la
otra combinación. La
desventaja de la reacción lenta
entre el sodio y el alcohol t-butílico (Sec.
18.4) en la
preparación del alcóxido
queda compensada por la
tendencia del halogenuro primario
a experimentar sustitución,
en vez de
eliminación. Al programa
una síntesis de
Williamson para un
dialquil éter, debemos
recordar siempre que la tendencia de
loos halogenuros de
alquilo a la
deshidrohalogenación es 3º >
2º > 1º.
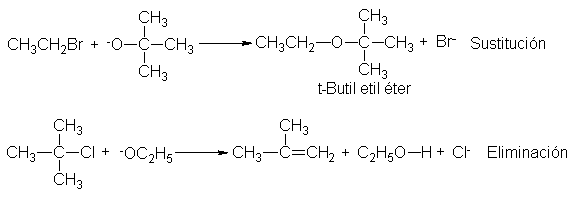
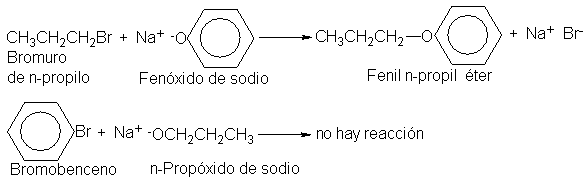
Para la
preparación de un alquil aril éter hay
también dos combinaciones a tener
en cuenta, pero
en general una puede rechazarse
de inmediato. Por ejemplos,
el fenil n-propil éter
únicamente puede prepararse
a partir del
halogenuro de alquilo
y el fenóxido
puesto que el
halogenuro de arilo
es muy poco
reactivo con los
alcóxidos.
Puesto que
los alcóxidos y fenóxidos
se preparan con los
alcoholes y fenoles
correspondientes, y los
halogenuros de alquilo
con alcoholes, la síntesis de
Williamson implica la
obtención de un
éter mediante dos alcoholes.