AMINAS http://organica1.org/qo1/ok/aminas/aminas.htm
Página principal http://organica1.org
Reducción de
nitrocompuestos
Al igual
que muchas otras
sustancias orgánicas, los
nitrocompuestos pueden reducirse
de dos maneras
generales: (a) por hidrogenación catalítica
usando hidrógeno molecular,
o (b) por
reducción química, habitualmente
con un metal y un ácido.
La hidrogenación
de un nitrocompuesto a
amina procede suavemente
cuando se agita
una solución del
nitrocompuesto en alcohol
con níquel o
platino finamente divididos
en una atmósfera
de hidrógeno. Por
ejemplo:

Este método
no puede emplearse
cuando la molécula
contiene algún otro
grupo fácilmente hidrogenable,
como un doble
enlace carbono-carbono.
 En laboratorio, la
reducción química se
efectúa muy a
menudo agregando ácido
clorhídrico a una
mezcla del nitrocompuesto con un
metal, en general
estaño granulado. En la
solución ácida, la
amina se obtiene
en forma de
sal, de la que se
libera por adición
de base y se destila
de la mezcla
mediante vapor. La
amina cruda suele
quedar contaminada con
algo del nitrocompuesto no
reducido, del que
puede separarse aprovechando
las propiedades básicas
de la amina; la
amina es soluble en
ácido mineral acuoso,
el nitrocompuesto, no.
En laboratorio, la
reducción química se
efectúa muy a
menudo agregando ácido
clorhídrico a una
mezcla del nitrocompuesto con un
metal, en general
estaño granulado. En la
solución ácida, la
amina se obtiene
en forma de
sal, de la que se
libera por adición
de base y se destila
de la mezcla
mediante vapor. La
amina cruda suele
quedar contaminada con
algo del nitrocompuesto no
reducido, del que
puede separarse aprovechando
las propiedades básicas
de la amina; la
amina es soluble en
ácido mineral acuoso,
el nitrocompuesto, no.
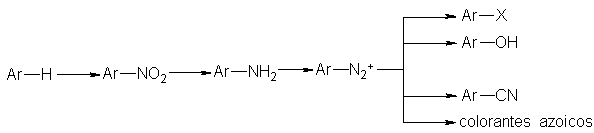
La reducción
de nitrocompuestos a aminas
es un paso
esencial en lo
que quizá sea
la vía de síntesis
más importante de
la química aromática.
Los nitrocompuestos se
preparan con facilidad
por nitración directa; cuando se
obtiene una mezcla
orto, para, estos suelen
ser separables y
pueden obtenerse en
forma pura. Las
aminas aromáticas primarias
resultantes de la
reducción de estos
nitrocompuestos se convierten
sin mayores problemas
en sales de
diazonio. A su
vez, el grupo diazo
de estas sales
es reemplazable por
muchos otros grupos.
En la mayoría
de los casos, esta
vía representa el
método más adecuado
para introducir estos
otros grupos en el anillo
aromático. Además, las
sales de diazonio
se emplean para
obtener un tipo
de compuestos de
gran importancia: los
colorantes azoicos.