AMINAS http://organica1.org/qo1/ok/aminas/aminas.htm
Página principal http://organica1.org
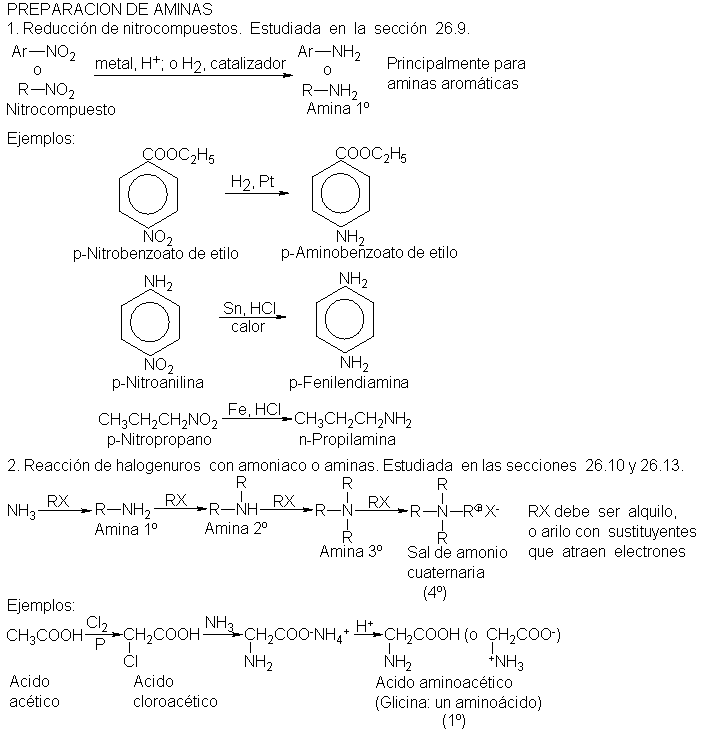
Preparación
Algunos de los
numerosos métodos utilizados
en el laboratorio
para preparar aminas se
ilustran en las
páginas siguientes:
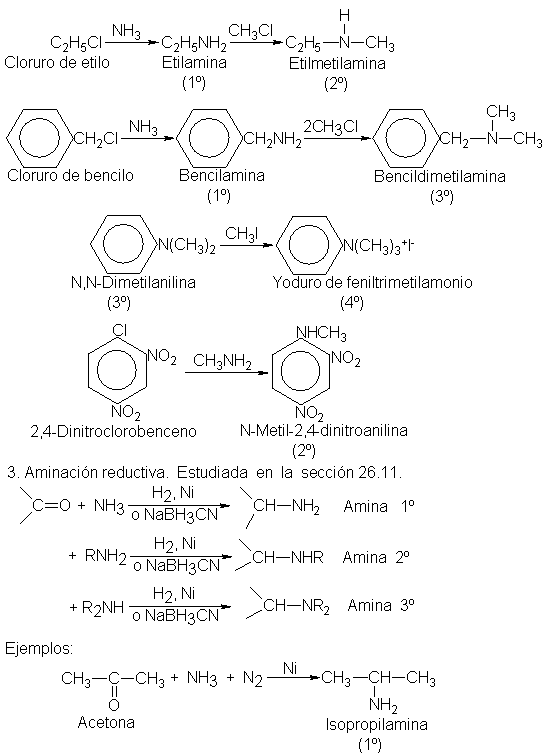
La
reducción de nitrocompuestos aromáticos
es el método
más útil para
preparar aminas, porque
utiliza materias fáciles
de adquirir y
genera el tipo
más importante de
aminas: las aminas
primarias aromáticas. Estas
pueden convertirse en
sales de diazonio
aromáticas que se
encuentran entre los
compuestos orgánicos más versátiles
conocidos. La secuencia
![]()
Proporciona la
mejor de las
vías para llegar
a docenas de
tipos de compuestos
aromáticos.
La reducción
de nitrocompuestos alifáticos
es limitada por
la disponibilidad de
materias primas.
Por lo
general, la amonólisis de
halogenuros queda circunscrita
a la serie
alifática, debido a
la escasa reactividad
de los halogenuros
de arilo ante
la sustitución nucleofílica.
Además, tiene la
desventaja de dar
una mezcla de
diferentes tipos de
aminas. Es importante
como método general
para introducir el
grupo amino (-NH2)
en moléculas diferentes;
por ejemplo, puede
emplearse para convertir
bromoácidos en aminoácidos.
La reacción exactamente
análoga, de halogenuros con
aminas, permite la
preparación de todos los
tipos de aminas
(así como sales
cuaternarias de amonio,
R4N+X-).
La aminación
reductiva, la reducción catalítica o química
de aldehídos (RCHO)
y cetonas (R2CO)
en presencia de amoniaco
o una amina, cumple prácticamente con
el mismo propósito
que la reacción
de los halogenuros,
ya que también
puede usarse para
preparar todo tipo de
aminas. Además, tiene
ciertas ventajas sobre
la reacción de
los halogenuros: la formación de
mezclas con la
aminación reductiva se
controla más fácilmente
que con la
amonólisis de halogenuros.
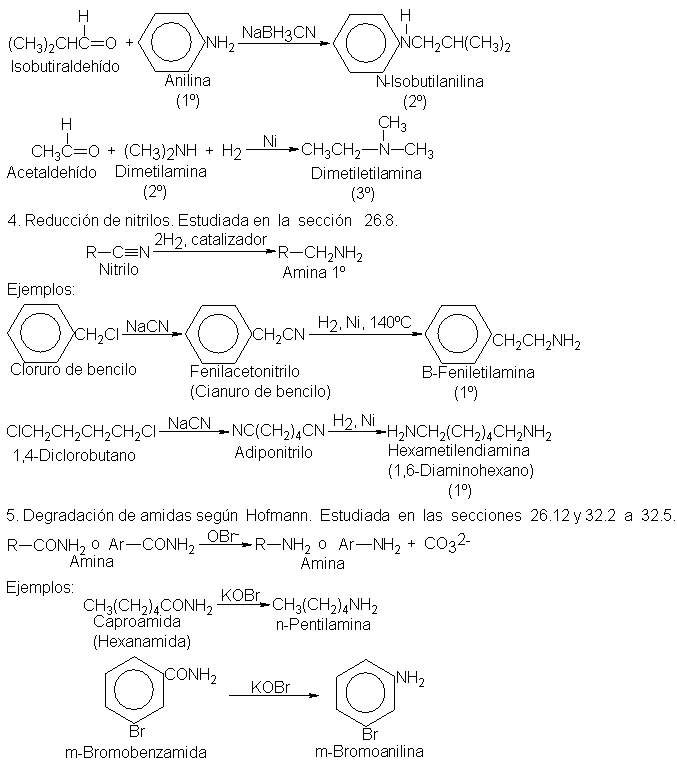
La aminación reductiva
de cetonas produce
aminas con un
grupo sec-alquilo; estas
son difíciles de
preparar por amonólisis,
porque la tendencia
de los halogenuros
de alquilo secundarios
es no experimentar
eliminación, sino sustitución.
La síntesis
por medio de
la reducción de
nitrilos tiene la
característica con un
especial de aumentar
la longitud de
una cadena carbonada,
generando una amina
primaria con un
átomo de carbono
más que el
halogenuro de alquilo del
cual se deriva.
La degradación de amidas,
según Hofmann, tiene
la propiedad de
disminuir la longitud
de una cadena
carbonada en un
átomo; también interesa como
ejemplo de un
tipo de reacciones
importantes que presentan
transposición.