AMINAS http://organica1.org/qo1/ok/aminas/aminas.htm
Página principal http://organica1.org
Propiedades físicas
de las aminas
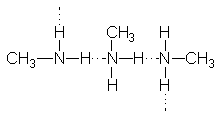 Como el
amoniaco, las aminas
son compuestos polares
y pueden formar
puentes de hidrógeno
intermoleculares, salvo las terciarias. Las
aminas tienen puntos
de ebullición más altos
Como el
amoniaco, las aminas
son compuestos polares
y pueden formar
puentes de hidrógeno
intermoleculares, salvo las terciarias. Las
aminas tienen puntos
de ebullición más altos
que los
compuestos no polares
de igual peso
molecular, pero inferiores
a los de
alcoholes o ácidos
carboxílicos.
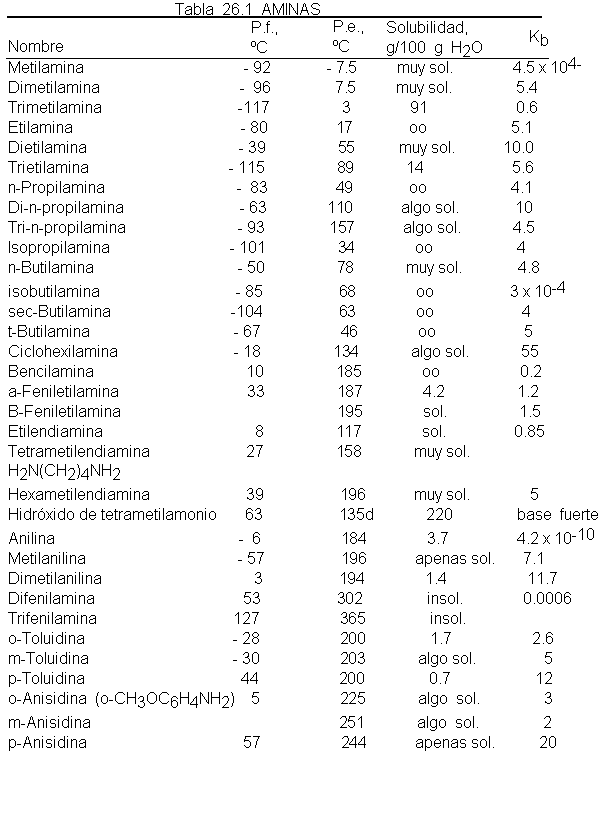

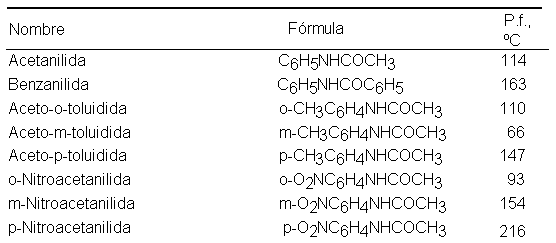
Los tres
tipos de aminas pueden
formar enlaces de
hidrógeno con el
agua. Como resultados,
las aminas menores
son bastantes solubles
en agua y
tienen solubilidad límite al
tomar unos seis
átomos de carbono. Son
solubles en disolventes
menos polares, como
éter, alcohol, benceno,
etc. Las metil y
etilaminas huelen muy
semejante al amoniaco.
Las alquilaminas superiores
tienen olor a
pescado en descomposición.
Las aminas
aromáticas suelen ser
muy tóxicas, ya
que son absorbidas
por la piel,
con resultados a
menudo fatales.
Las aminas
aromáticas se oxidan
fácilmente al aire
y con frecuencia
se las encuentra
coloreadas por productos
de oxidación, aunque
son incoloras cuando
están puras.