Página
principal http://organica1.org
8 Oxidación
Los aldehídos
se oxidan con
facilidad a ácidos
carboxílicos, no así las
cetonas. La oxidación,
que se debe
a la diferencia
en sus estructuras,
es la reacción
que más distingue
a los aldehídos
de las cetonas;
por definición, un
aldehído tiene un
átomo de hidrógeno
unido al carbono
carbonílico, el cual
no aparece en una
cetona. Cualquiera que
sea el mecanismo
exacto, este hidrógeno
es sustraído durante
la oxidación, bien
como un protón
o como un
átomo, mientras que
la reacción análoga
para una cetona
no tiene lugar:
la separación de un grupo
alquilo o arilo.
Los aldehídos
no sólo son oxidados
por los mismos
reactivos que oxidan
alcoholes primarios y
secundarios permanganato y dicromato, sino también
por el débilmente
oxidante ión plata.
La oxidación por
ión plata requiere
un medio alcalino,
y para evitar
la precipitación del
óxido de plata
insoluble se añade
un agente completamente: amoniaco.
El
reactivo de Tollens
contiene el ión
diaminaplata, Ag(NH3)2+. La
oxidación del aldehído
va acompañada por
reducción del ión
plata a plata
elemental (en forma
de espejo, si
las condiciones son
las adecuadas).
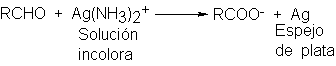
(La oxidación
con ión cúprico
complejo es una característica de ciertos compuestos
carbonílicos sustituidos y se tratará junto
con los carbohidratos en )
La oxidación
con el
reactivo de Tollens
es útil en
la detección de
aldehídos, en particular
para diferenciarlos de las .
Esta reacción es
de utilidad en
síntesis donde los
aldehídos son más
accesibles que los
ácidos correspondientes; en
especial en las
síntesis de ácidos
no saturados con aldehídos
no saturados obtenidos
mediante la condensación
aldólica , donde se
aprovecha el hecho
de que el
reactivo de Tollens
no ataca dobles
enlaces carbono-carbono.

La oxidación
con el reactivo
de Tollens es
útil en la
detección de aldehídos,
en particular para
diferenciarlos de las
cetonas. Esta reacción
es de utilidad
en doble enlace
de la forma
enólica y, donde
la estructura lo
permite, tiene lugar
a
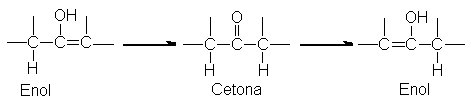
Ambos lados
del grupo carbonilo.
Por tanto, es
habitual obtener una
mezcla de ácidos
carboxílicos.
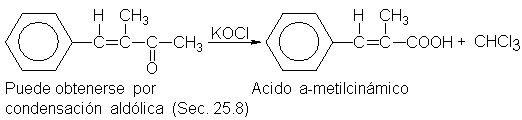
Las metilcetonas se oxidan
suavemente por medio
de un hipohalogenito en
la reacción del
haloformo. Aparte de
utilizarse a menudo
para detectar estas
cetonas, la reacción
mencionada también es
útil en síntesis,
donde el hipohalogenito tiene
la ventaja especial
de no atacar
dobles enlaces carbono-carbono. Por ejemplo: