Página
principal http://organica1.org
9 Análisis
de alcoholes. Caracterización. Prueba
del yodoformo
Los
alcoholes se disuelven en
ácido sulfúrico concentrado, propiedad que
comparten con alquenos, aminas, prácticamente
todos los compuestos que
contienen oxígeno y con los
compuestos que se
sulfonan fácilmente. (Al
igual que otros
compuestos oxigenados, los
alcoholes forman sales
de oxonio, que se disuelven
en el ácido
sulfúrico muy polar.)
Los alcoholes
no son oxidados
por el permanganato
frío, diluido y
neutro (los alcoholes
primarios y secundarios,
evidentemente, son oxidados
por el permanganato
en condiciones más
vigorosas). Sin embargo,
hemos dicho que
los alcoholes a
menudo contienen impurezas
que son oxidadas en
estas condiciones, lo
que la prueba
del permanganato debe ser
interpretada en cierta cautela.
Los alcoholes
no decoloran la solución
de bromo en tetracloruro de
carbono, propiedad que
permite distinguirlos de
alquenos y alquinos.
Además, los alcoholes
se pueden diferenciar
de alquenos y
alquinos y de
casi todos los
demás tipos de compuestos
por la oxidación
con anhídrido crómico,
CrO3, en ácido sulfúrico
acuoso: en dos segundos,
la solución transparente
anaranjada se vuelve
azul verdosa y opaca.
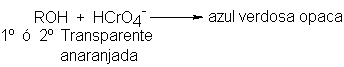
Los alcoholes
terciarios no dan
esta prueba. Los
aldehídos sí la dan,
pero se pueden
diferenciar fácilmente con
otros ensayos
La reacción
de los alcoholes son
sodio metálico, produciendo
hidrógeno gaseoso, sirve
para caracterizarlos; sin
embargo, es evidente que
cualquier compuesto húmedo hará
lo mismo, hasta
haber consumido el agua.
A menudo
se detecta la presencia
del grupo OH
en una molécula
por la formación
de un éster
después del tratamiento
con un cloruro
o anhídrido de ácido. Algunos ésteres
tienen olores dulces, otros
son sólidos con
puntos de fusión muy
definidos, por lo
que pueden emplearse
para fines de
identificación. (Si se
determinan las fórmulas
moleculares de los materiales originales y
de los productos,
es posible calcular
cuántos grupos OH
hay presentes.)
La prueba
de Lucas indica
si se trata
de un alcohol
primario, secundario o
terciario, y se
basan en la
diferencia de reactividad
de los tres
tipos con los
halogenuros de hidrógeno.
Los alcoholes (de no
más de seis carbonos) son solubles
en el reactivo de Lucas, que
es una mezcla que
en agua?) Los cloruros de alquilo correspondientes son
insolubles. La formación de un cloruro,
a partir de
alcohol, se manifiesta
por la turbiedad que
aparece cuando se
separa el cloruro
de la solución; en consecuencia, el
tiempo que transcurra
hasta la aparición de la turbiedad
es una medida
de la reactividad
del alcohol.
Un
alcohol terciario reacciona
de inmediato con el
reactivo de Lucas, mientras
que uno secundario reacciona
en cinco minutos; a
temperatura ambiente, un
alcohol primario no reacciona
de forma apreciable.
El alcohol alílico reacciona
tan velozmente como
los alcoholes terciarios
con el reactivo de Lucas; sin
embargo, el cloruro
de alilo es
soluble en el
reactivo. (¿Por qué?)
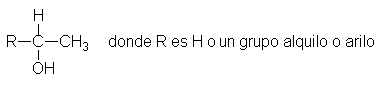 La prueba del yodoformo indica si un
alcohol contiene o no
una unidad estructural determinada. Se
trata de alcohol
con yodo e hidrógeno
de sodio (hipoyodito de
sodio, NaOI); un alcohol de
estructura
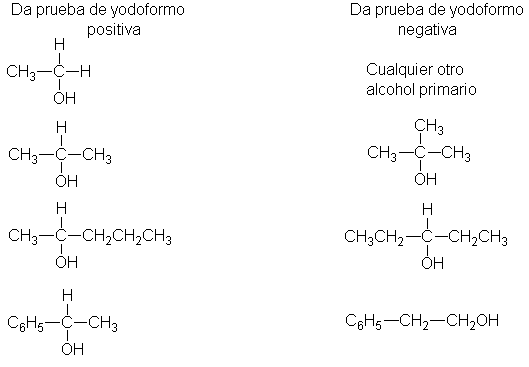
La prueba del yodoformo indica si un
alcohol contiene o no
una unidad estructural determinada. Se
trata de alcohol
con yodo e hidrógeno
de sodio (hipoyodito de
sodio, NaOI); un alcohol de
estructura
Da un precipitado
amarillo de yodoformo
(CHI3, p.f. 119ºC).
Por ejemplo:
La reacción
comprende oxidación, halogenación
y degradación.
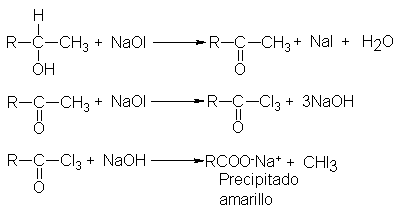
Como es de
suponer a partir
de las ecuaciones, un
compuesto de estructura
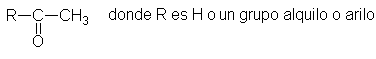
También da
una prueba positiva.
En ciertos
casos especiales, esta reacción
no se emplea
como ensayo, sino
para sintetizar ácidos
carboxílicos, RCOOH. Aquí
probablemente se utilizaría
hipobromito, o hipoclorito,
que es más
barato.