Página principal http://organica1.org
Acidez de
ácidos carboxílicos
Veamos ahora
cómo se relaciona
la acidez de
ácidos carboxílicos con sus
estructuras respectivas. Al
hacerlo, supondremos que
la acidez está
determinada principalmente por
la diferencia de estabilidad entre
el ácido y su unión.
En primer lugar,
y lo más
importante, está el
hecho de que
los ácidos carboxílicos
son con certeza
ácidos. ¿Cómo explicaremos,
por ejemplo, que
el OH de
un ácido carboxílico
tiende a liberar
un ión hidrógeno
con mayor facilidad
que el OH
de un alcohol? Examinemos las
estructuras de reactivos
y productos para
los dos casos.
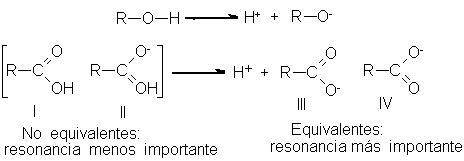
Se bserva
que el alcohol
y el ión
alcóxido se representa
satisfactoriamente por una
sola estructura. En
cambio, desarrollamos dos
estructuras razonables ( I y
II) para el
ácido carboxílico, y
también dos para
el anión carboxilato
(III y IV):
ambos son híbridos
de resonancia. Pero,
¿es igualmente importante
la resonancia en
los dos casos?
Sabemos que la
resonancia es mucho
más importante entre
estructuras equivalentes, como
III y IV,
que entre estructuras
no equivalentes, I y
II. Así
pues, a pesar
de que ácido
y anión se
estabilizan por resonancia
la estabilización es
mucho mayor para el
anión que para
el ácido. El
equilibrio se desplaza
en la dirección
de la ionización
mayor, y aumenta
Ka.
En rigor,
es más correcto
decir que la
resonancia es menos
importante para el
ácido porque las
estructuras contribuyentes son
de estabilidad diferente,
mientras que las
equivalentes para el
ión deben ser
necesariamente de igual
estabilidad. En la
estructura II, dos
átomos de electronegatividad similar
portan cargas opuestas;
como es necesario
aplicar energía para
separar cargas opuestas,
II debería ser
más energética, y
por tanto menos
estable que I.
La consideración de
la separación de
cargas es una
de las reglas
empíricas que pueden
utilizarse para estimar
la estabilidad relativa y, en consecuencia,
la importancia relativa
de una estructura
contribuyente.
Por consiguiente,
la acidez de un
ácido carboxílico se debe
a la fuerte
estabilización por resonancia
de su anión.
Esta estabilización y la acidez
resultante sólo son
posibles por la
presencia del grupo
carbonilo.