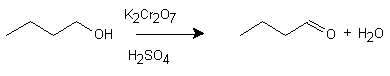
PRACTICA VI
OXIDACION DE n-BUTANOL a n-BUTIRALDEHIDO
a) Ejemplificar un método para obtener aldehídos alifáticos mediante la deshidrogenacion de alcoholes.
b) Formar un derivado sencillo del aldehído obtenido para caracterizarlo.
REACCION
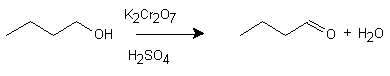
II. MATERIAL
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
2 |
|
1 |
|
3 |
|
1 |
|
1 1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
1 |
|
2 |
|
1 |
III. SUSTANCIAS
|
1.9 g |
|
2.0 ml |
|
0.5 ml |
|
2.0 ml 1.6 ml |
IV. INFORMACION
a) La oxidación de alcoholes a aldehídos o cetonas es una reacción de eliminación muy útil. El ácido crómico y diversos complejos de CrO3 son los reactivos más útiles en los proceso de deshidrogenación en el laboratorio.
b) En el mecanismo de eliminación con ácido crómico se forma inicialmente un ester crómico el cual experimenta despues una eliminación 1,2 produciendo el doble enlace del grupo carbonilo.
c) Los aldehídos son compuestos con punto de ebullición menor que el de los alcoholes y de los ácidos carboxílicos con peso molecular semejantes.
V. PROCEDIMIENTO
A un matraz pera de dos bocas adapte por una de ellas, un embudo de adición y por la otra un sistema de destilación fraccionada con una columna Vigreaux.
En un vaso de precipitado disuelva 1.9 g de dicromato de potasio dihidratado en 12.5 ml de agua, añada cuidadosamente y con agitación 1.3 ml de ácido sulfúrico concentrado (Nota 1).
Adicione 1.6 ml de n-butanol al matraz pera, en el embudo de separación coloque la solución de dicromato de potasio-ácido sufúrico. Caliente a ebullición el n-butanol con flama suave usando un baño de aire, de manera que los vapores del alcohol lleguen a la columna de fraccionamiento. Agregue entonces, gota a gota, la solución de dicromato de potasio-ácido sulfúrico en un lapso de 15 minutos (Nota 2), de manera que la temperatura en la parte superior de la columna no exceda de 80-85oC (Nota 3).
Cuando se ha añadido todo el agente oxidante continue calentando la mezcla suavemente por 15 min. más y colecte la fracción que destila abajo de los 90oC (Nota 4).
Pase el destilado a un embudo de separación (limpio), decante la fase acuosa y mida el volumen de butiraldehído obtenido para calcular el rendimiento.
Agregue dos gotas del producto a 0.5 ml de una solución de 2,4- dinitrofenilhidrazina en un tubo de ensayo y agite vigorosamente; al dejar reposar precipita el derivado del aldehído el cual puede purificar por cristalización de etanol-agua. El punto de fusión reportado para la 2,4-dinitrofenilhidrazona del butilraldehído es de 122oC.
NOTAS
1) !PRECAUCION! La reacción es exotérmica. Cuando se enfría la solución, el dicromato cristaliza, de ser así, caliente suavemente con flama y pásela al embudo de separación en caliente. Continúe con la técnica.
2) Más o menos dos gotas por segundo.
3) La deshidrogenación del alcohol se efectua con producción de calor, pero puede ser necesario calentar la mezcla de vez en cuando para que la temperatura no baje de 75oC.
4) La probeta en la que reciba el destilado debe estar en baño de hielo.
VI. ANTECEDENTES
a) Oxidación. Diferentes agentes oxidantes. Acción sobre alcoholes y grupo carbonilo de aldehídos y cetonas.
b) Método de obtención de aldehídos y cetonas.
c) Propiedades físicas, químicas y toxicidad de los reactivos y productos .
d) Principales derivados de aldehídos y cetonas usados en su caracterización (reactivos y reacciones).
VII. CUESTIONARIO
1) ¿Cuál es la finalidad de hacer la mezcla de dicromato de potasio, agua y ácido sulfúrico?
2) Explique como evita que el butiraldehidro obtenido en la práctica se oxide a ácido
3) ¿Cómo puede comprobar que obtuvo butiraldehído en la práctica?
4) ¿Cómo deben desecharse los residuos de sales de cromo?
5) Asigne las bandas principales a los grupos funcionales presentes en los espectros de I.R. de reactivos y productos.
Espectros de I.R.
a) n-butanol
VII. BIBLIOGRAFIA
a) Vogel A.I.
Text-book Practical Organic Chemistry
4rd Edition
Longmans, London (1978).
b) R.T. Morrison y R.N. Boyd.
Química Orgánica
2a. Edición
Fondo Educativo Interamericano S.A.
México (1985).
c) Brieger, G.
Química Orgánica Moderna
Curso Práctico de Laboratorio
Ediciones del Castillo, S.A.
Madrid (1970).
Diagrama de flujo de tratamiento de residuos